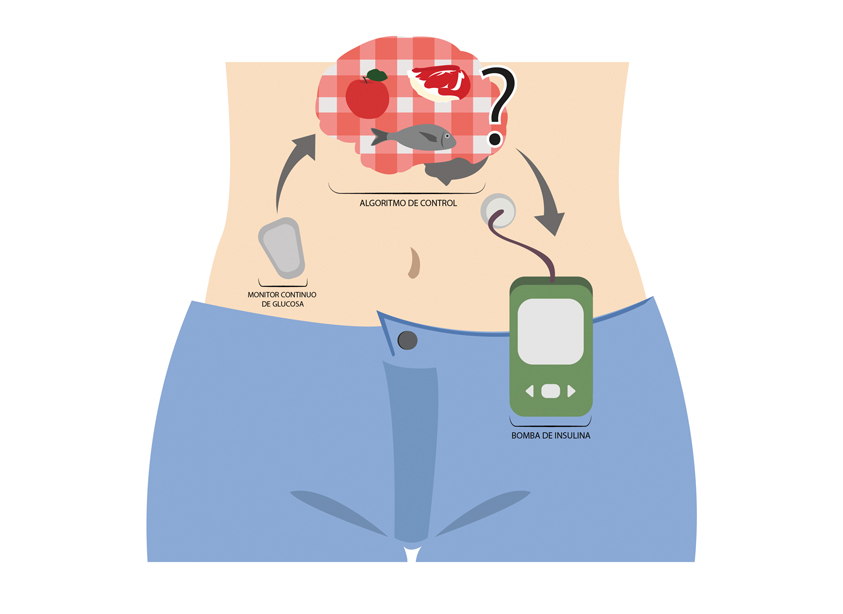
El momento de la comida es de especial significancia para un buen control de la diabetes y no es menos para un páncreas artificial. ¿Debe conocer el páncreas artificial cuándo comemos y qué comemos? En un páncreas artificial híbrido la respuesta es sí. De la misma forma que ahora se debe administrar en el momento de la comida un bolo de insulina en base a las raciones de hidratos de carbono estimadas, entre otras cosas, en un páncreas artificial híbrido el paciente debe informar al sistema sobre la comida. Es decir, siguen habiendo bolos de insulina manuales con la intervención del paciente. Actualmente, la gran mayoría de sistemas de páncreas artificial en desarrollo son híbridos.
El mayor desafío del control de glucosa en las comidas es que la absorción de las insulinas actuales es demasiado lenta comparado con el efecto de la comida.
Cuando se inyecta la insulina, se produce un depósito bajo la piel que empieza a difundirse mientras las moléculas de insulina, que inicialmente están agrupadas, se van desagrupando y entran en la sangre. Desde allí se distribuye hasta su lugar de acción: el hígado, disminuyendo su producción de glucosa, y el músculo y la grasa, aumentando su consumo de glucosa. Con ello, la insulina baja la glucosa en sangre. Todo este proceso puede tardar unos noventa minutos. Si el sistema de páncreas artificial desconoce que se ha comido, reaccionará aumentanto la insulina cuando mida que la glucosa se está desviando de su objetivo por efecto de la comida, pero será demasiado tarde para evitar valores altos de glucosa.
Las desventajas son muchas comparado con un páncreas sano. Por una parte, el páncreas sano secreta insulina directamente en sangre y tarda sólo unos treinta minutos en actuar, comparado con los noventa minutos anteriores. Por otra parte, el páncreas sano incluso empieza a secretar insulina antes de empezar a absorber la comida (lo que se conoce como “fase cefálica”). Llevar la cuchara a la boca ya incita al páncreas a trabajar. La aparición de insulinas con una absorción mucho más rápida que las actuales será fundamental para pasar de un páncreas artificial híbrido a uno totalmente automático, igualmente eficiente, sin necesidad de intervención del paciente en el momento de la comida. Éste es un área muy activa de investigación en la industria farmacéutica.
¿Quieres conocer más? No te olvides de seguirnos y transmitirnos tus dudas e intereses.
Referencias bibliográficas:
Weinzimer, S. A., Steil, G. M., Swan, K. L., Dziura, J., Kurtz, N., & Tamborlane, W. V. (2008). Fully automated closed-loop insulin delivery versus semiautomated hybrid control in pediatric patients with type 1 diabetes using an artificial pancreas. Diabetes Care, 31(5), 934–939.
Hovorka, R. (2006). Continuous glucose monitoring and closed-loop systems. Diabetic Medicine, 23(1), 1–12.
Foto: Daniel Costa, Instituto ai2, Universitat Politècnica de València